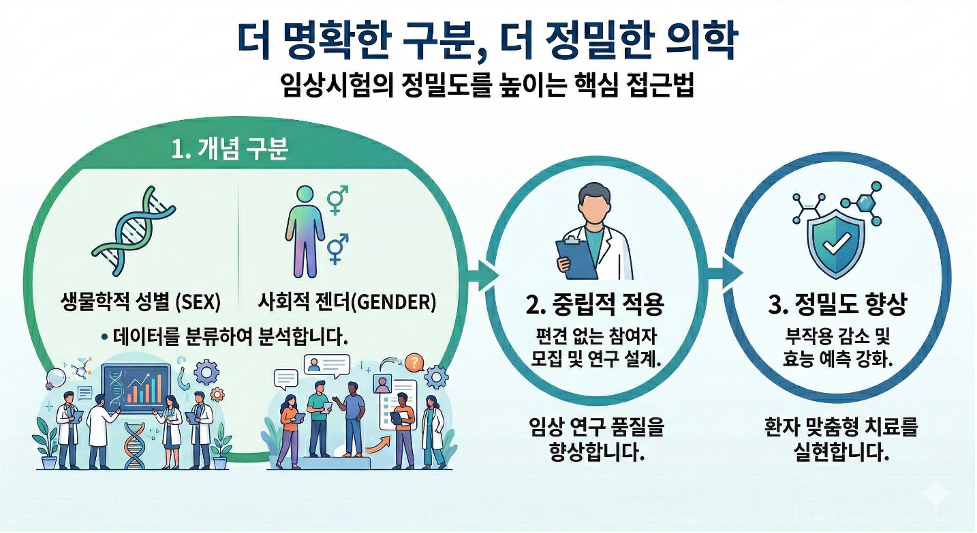
임상시험의 과학적 정밀도를 높이는 성별(sex)과 젠더(gender) 구분
혼용되는 두 개념이 초래하는 데이터 공백
최근 임상시험에서 생물학적 ‘성별(sex)’과 사회적 ‘젠더(gender)’를 명확히 구분해 데이터에 반영하는 것을 핵심 설계 요소로 주목하고 있습니다. 성별이 유전적·호르몬적 특성에 기반한 생물학적 지표라면, 젠더는 개인이 사회문화적 맥락 속에서 경험하는 정체성과 성 역할, 행동 양식을 포괄하는 개념입니다.
한 연구[i]는 ClinicalTrials.gov에 등록된 임상연구를 대상으로, 실제로는 ‘출생 성별(Sex)’에 기반한 대상자 기준을 사용하면서도 ‘Gender eligibility’로 잘못 보고한 사례가 2/3에 이른다고 분석하였습니다. 이러한 보고 오류는 성별과 젠더를 하나의 항목으로 결합하여 기록하도록 되어 있었던 등록 시스템 구조와 연구자들의 개념 이해 부족에서 비롯되었다고 지적하였습니다.
두 요소를 구분하여 주의 깊게 사용하지 않을 경우, 결과적으로 특정 인구 집단에 대한 데이터 공백(data gap) 또는 혼합(data blending)이 발생될 수 있습니다.[ii] 이는 목표 질병의 인구구조를 제대로 반영하지 못하거나 소수 집단의 참여 여부를 파악하지 못하는 결과로 이어져, 결과적으로 충분히 대표되지 못한 집단의 건강 불평등이 심화되고 임상연구의 과학적 신뢰성이 훼손될 수 있습니다.
성별과 젠더 요소의 임상연구 반영 전략
생물학적 특성에 기반한 성별은 약물의 약동학, 약력학, 질환의 발생 양상 등에 영향을 미칠 수 있고, 젠더는 의료 접근성, 건강 관련 행동 양식, 치료 순응도와 같은 사회적 요인과 보다 밀접하게 관련되어 있습니다. 이러한 차이는 서로 다른 방식으로 임상연구 과정에 영향을 미치기 때문에, 임상시험 설계부터 대상자 모집, 운영 및 데이터 분석과정까지 두 개념을 명확히 구분하여 적용하는 것이 중요합니다.
- 성별 대표성 확보를 위한 임상설계: 모집계획 및 통계적 설계
임상시험 설계 단계에서 질환의 성별간 유병률 차이를 고려하여, 가능한 범위 내에서 성별 대표성을 확보하는 모집 전략과 대상자 구성을 계획합니다. 특정 성별에 편중되지 않도록 모집 채널을 다양화하고, 성소수자 집단을 포함한 다양한 집단의 참여를 유도하는 방안도 함께 고려할 수 있습니다.
초기 임상시험이거나 성별이 결과 변수에 주된 영향을 미치는 예후 요인(prognostic factor)이라면, 성별을 무작위배정 층화 변수(stratification variable)로 반영하여 시험군 간 성별 분포의 불균형을 줄이도록 설계하고 통계 분석 계획에 반영합니다. 또한 성별 하위군 분석(subgroup analysis)을 사전에 계획하여, 성별에 따른 유효성과 안전성 차이를 확인할 통계적 검정력을 확보하는 접근도 유용합니다.
- 데이터 수집: 용어의 정교화와 ‘중립적 질문방법’
대상자 모집 및 선정 기준 등 데이터 수집 과정에서 성별과 젠더를 구분하여 중립적으로 질문합니다. ‘출생 시 성별(Sex assigned at birth)’과 ‘현재 인지된 젠더 정체성(current gender identity)’을 가능하면 함께 확인하고, 성별 데이터만 수집시에는 ‘출생 시 성별’임을 명확히 합니다.
중립적인 질문의 예로, 임상시험 대상자와 파트너의 가임력에 관한 질문을 할 때, 성별에 따른 질문 구조(예: 여성의 경우 가임기 여부, 남성의 경우 남성불임 여부를 묻는 방식) 대신, 성별·젠더 중립적 구조(예: “대상자가 의학적으로 임신 또는 임신 유발이 가능한 상태입니까?”)를 사용하는 것이 권장됩니다. 이처럼 솔직한 답변을 유도하는 질문법은, 호르몬 요법이 약물 반응에 미치는 영향 등 복합적인 변수 해석에서 성별 및 젠더가 함께 고려되어야 할 경우 더욱 필수적입니다.
- 연구 운영 전략: 참여 장벽 완화를 위한 고려
사회적 역할(돌봄 책임, 직업적 환경 등) 또는 경제적으로 제한된 지위로 인한 연구 참여 장애 요인을 최소화할 수 있는 유연한 운영 전략을 도입해야 합니다.
주말·야간 방문 허용 및 방문 서비스 지원을 통해 사회경제적 차이로 인한 참여 격차를 해소하고, 병원 방문 부담을 줄일 수 있는 분산형 임상시험(DCT, Decentralized Clinical Trial) 기술에 기반한 원격 방문 및 웨어러블 기기의 활용을 적극 고려합니다.
- 분석 및 결과 보고: 하위군 분석의 투명한 공개
성별에 따른 유효성과 안전성에 있어 통계적 유의미한 차이가 발견되지 않은 경우에도, 하위군 분석 결과를 투명하게 공개하는 것이 SAGER(Sex and Gender Equity in Research) 지침에 따라 권장됩니다. 미국 FDA 가이드라인[iii] 역시 성별에 따른 임상 결과를 의약품·기기 제품 라벨에 포함할 것을 요구하고 있으며, 국내에서도 식약처(MFDS)가 의약품 임상시험 계획서 작성 가이드라인을 통해 성별 하위군 분석 계획의 사전 수립을 권고하고 있습니다.
이러한 노력은 후속 연구자들에게 중요한 메타데이터를 제공하고, 임상 현장에서 성별과 젠더 정체성이 건강과 치료 결과에 미치는 영향을 반영하여 환자별 맞춤 처방을 가능하게 하는 근거가 될 것입니다.
임상연구의 정밀도 향상을 위한 진보
임상시험에서 성별과 젠더를 함께 고려하는 것은 단순한 변수 추가가 아니라, 인간의 생물학적 본질과 사회적 맥락을 통합적으로 이해하고 연구 과정 전반에 반영하려는 노력입니다. 예를 들어, 통증 및 우울증 관련 분자 경로 연구[iv]에서 성별에 따른 차이가 확인되어 새로운 표적 치료의 방향이 제시된 바 있습니다. 이처럼 성별·젠더를 통합적으로 고려하는 접근은 다양한 환자 집단에 대한 치료 효과와 안전성을 보다 정확하게 이해하고, 정밀 의료(Precision Medicine)의 실현을 앞당기는 데 기여할 것입니다.
[i] Burton A, Mohan S, Puplampu-Dove Y, Tse T. Characterizing gender eligibility descriptions for clinical trials registered on ClinicalTrials.gov. JAMA. 2023;330 (20):2019-2021. doi:10.1001/jama.2023.19517
[ii] Tannenbaum, C., et al. Sex and gender analysis improves science and engineering. Nature. 575, 137–146 (2019)
[iii] US FDA Guidance, Study of Sex Differences in the Clinical Evaluation of Medical Products, https://www.fda.gov/regulatory-information/search-fda-guidance-documents/study-sex-differences-clinical-evaluation-medical-products
[iv] Mogil JS. Sex differences in pain and pain inhibition: multiple explanations of a controversial phenomenon. Nature Rev Neuroscience. 2012;13:859–66.
김재명 | EVP
본고는 작성자 개인의 내용, 구성 및 편집 방향에 대한 의견에 따라 다양한 관점을 소개하기 위한 것이며, 당사의 공식 의견을 대변하지 않습니다.